1――原則的な値段の決め方
まず、原則的な価格設定についてみていきましょう。できるだけ簡単に紹介していきます(*1)。
(*1) 本稿は、「薬価算定の基準について」(厚生労働省保険局長通知, 保発02077 第1 号, 平成30 年2月7日)や、「薬事ハンドブック2018」(じほう) などを参考に、執筆しています。
1|医療用医薬品には、公定価格である薬価が定められています
日本では、医薬品は、大きく、保険適用となる医療用医薬品と、保険適用にならない一般用医薬品に分けられます(*2)。このうち、医療用医薬品については、全国一律の公定価格である、薬価が定められています。一方、一般用医薬品は、一般の物品・サービスと同様に、自由価格となっています。
(*2) このほかに、薬局製剤や要指導医薬品があります。薬局製剤は、薬局の調剤室で、薬剤師が薬剤を製造するものです。要指導医薬品は、以前は医療用医薬品だったものが、一般用医薬品に移行する際の、途中段階のもの(スイッチ直後品目)や、医療用医薬品としての使用経験がないまま販売が承認されたもの(ダイレクトOTC)、更には毒性・劇性を持つ劇薬です。いずれも保険適用にはならず、値段は自由価格です。
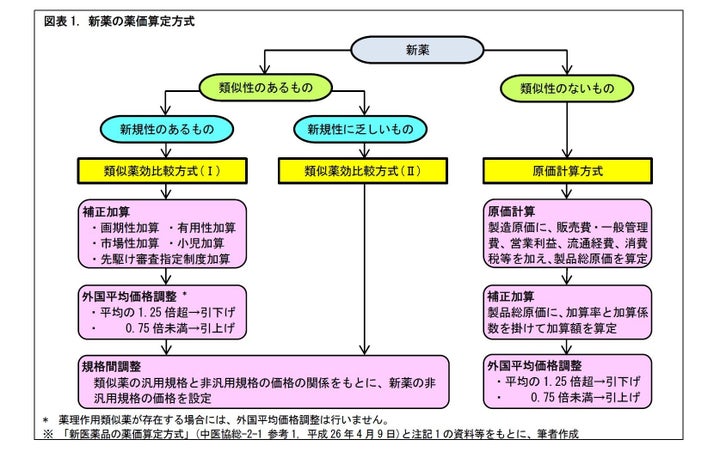
2|新薬の薬価の設定方法には、2つの方式があります
新薬の薬価設定には、「類似薬効比較方式」と「原価計算方式」の2つの方式があります。既存の新薬との類似性の有無に応じて、どちらの方式をとるかが決まります。
(1) 類似薬効比較方式
既存の新薬と類似性のある新薬を開発する場合は、類似薬効比較方式がとられます。
新薬に新規性があれば、既存新薬の薬価に、補正加算として、画期性、有用性、市場性に応じた加算や、小児加算、先駆け審査指定制度加算を行います。
その上で、アメリカ、イギリス、ドイツ、フランスにおける価格の平均額との乖離が大きい場合、その平均額を踏まえて外国平均価格調整(*3),(*4)を行います。ただし、薬理作用類似薬(*5)が存在する場合には、この調整は行いません。
一方、新薬が新規性に乏しい場合は、補正加算や外国平均価格調整は行いません(*6)。
そして、類似薬の汎用規格と非汎用規格の価格の関係をもとに、新薬について汎用規格の価格から非汎用規格の価格を設定する規格間調整と呼ばれる調整を行います。
(*3) 次に該当する場合は、当該価格を外国平均価格とします。①価格が2カ国以上あり、最高価格が最低価格の2.5倍を上回る場合は、当該最高価格を除外して平均した額、②価格が3ヵ国以上あり、そのうち最高価格がそれ以外の価格の平均額の2倍を上回る場合は、当該最高価格をそれ以外の価格の平均額の2倍相当とみなして平均した額。
(*4) 2018年の薬価改定で、アメリカについては、従来参照してきたRed Bookというメーカー希望小売価格のリストの代わりに、公的制度(メディケア・メディケイド)で用いられている価格リスト(ASP/NADAC)が参照されることとなりました。
(*5) 効能・効果・投与形態が同一で、効能・効果に関する薬理作用が類似している既存の薬(薬価収載された薬)のこと。
(*6) 「新規性に乏しい」とは、薬理作用類似薬が3つ以上存在する場合をいいます。
(2)原価計算方式
既存の新薬とは類似性のない新薬を開発する場合は、原価計算方式がとられます。
この方式では、原材料費、労務費、製造経費から製造原価を算定します。これに、販売費・一般管理費、営業利益(*7)、流通経費、消費税等を上乗せして製品総原価が算定されます。各費目の計算に用いる係数は、原則、前年度末時点で取得できる直近3ヵ年の医薬品製造業の実績平均の値とされます。
その上で、補正加算が行われます。加算額は、製品総原価に、加算率と加算係数を掛け算した額です。加算率は、新薬開発のイノベーションを評価するもので、その要件や水準は類似薬効比較方式を準用して0~120%の範囲内で決まります。
一方、加算係数は、経費の薬価算定組織への情報開示度が低い場合に補正加算を抑制する仕組みで、製品総原価中の開示可能部分の割合に応じて1、0.6、0.2のいずれかの値となります(*8)。
最後に、外国平均価格調整が行われます。
(*7) 営業利益の計算に用いる営業利益率には、既存治療と比較した場合の革新性の程度に応じて、平均的な営業利益率の-50%~0%の範囲内の値が用いられます。(注記1に記載の通知より)
(*8) 開示度が80%以上の場合は1、50%以上80%未満の場合は0.6、50%未満の場合は0.2とされています。
3|設定された薬価は、薬価改定で見直されます
通常、医薬品は、医薬品メーカーから、医薬品卸事業者を通じて、医療機関、保険薬局に販売されています。医薬品卸事業者と医療機関、保険薬局との間で取引される際の価格(実勢価格)は、当事者間の交渉で決まります。そのため、薬価と実勢価格の間には乖離が生じます。その乖離を小さくするために、定期的に薬価改定が行われます。
通常、時間が経つに連れて、実勢価格は下がっていきますので、薬価改定により、薬価は引き下げられることが一般的です。薬価改定の前年には、実勢価格を把握するために、薬価調査が行なわれます。
従来、薬価改定は診療報酬の改定と同様、2年に一度行われてきました。しかし、一部の医薬品では、2年の間に薬価と実勢価格の乖離が大きくなっていました。
そこで、実勢価格を薬価にタイムリーに反映する観点から、全品目を対象に毎年薬価調査を行い、乖離の大きい品目については中間年にも薬価改定を行うこととなりました。2020年中に、中間年改定の対象範囲が設定される見通しです(*9)。
(*9) 中間年の薬価調査は、全ての医薬品卸事業者を対象に実施するものの、全数調査ではなく、医薬品卸事業者ごとに一部の営業所を抽出する調査となる予定です。
2――値段の決め方の特例
医薬品の値段の設定には、いくつかの特例があります。主な特例を、簡単にみていきましょう。
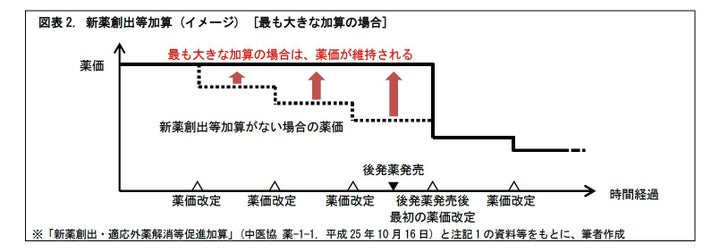
1|革新的な新薬は、薬価改定時に加算が行われて薬価が維持されます
革新的な新薬は、医療の質を高め、患者の負担を軽減する可能性があります。医薬品メーカーに革新的な新薬の創出を促すために、薬価改定の際に、医薬品の革新性・有用性に応じて、「新薬創出・適応外薬解消等促進加算」(通称、「新薬創出等加算」)と呼ばれる加算が行われています。
加算は、医薬品メーカーが、革新的新薬創出、ドラッグ・ラグ対策(*10)、世界に先駆けた新薬開発を行っているかという点を企業指標として、その達成や充足の状況に応じて行われます。
加算対象の医薬品は、ジェネリック医薬品未発売かつ薬価収載後15年未満のもので、革新性・有用性に着目して判断されます。最も大きな加算が適用される医薬品メーカーの場合は、薬価改定時に薬価が維持されます(*11)。
この加算は、2010年に試行導入され、医薬品メーカーは、加算の恒久化・制度化を求めてきました。2018年の薬価改定では、制度化の検討とともに、加算対象となる品目要件の厳格化が図られ、対象品目の絞り込みの議論が進められました。
(*10) ドラッグ・ラグは、海外で導入済みの新薬が日本で販売されない期間を指します。特許期間中に薬価が下がると、新薬メーカーの日本での開発意欲が失われる恐れがあるため、その対策として、新薬創出等加算が行われているという側面があります。
(*11) 2018年の改定では、加算が薬価を維持する場合の0.9倍、0.8倍にとどまる医薬品メーカーの区分が設けられました。
2|特別に薬価の引下げが行われることがあります
新薬が想定以上に売れたり、用法や用量に変更があったりした場合には、薬価の引き下げが行われることがあります。
(1) 市場拡大再算定
薬価の見直しは、薬価改定で行われることが原則です。しかし、販売後に、新薬が想定以上に売れると、特別に薬価の引下げが行われることがあります。これは、「市場拡大再算定」と呼ばれます(*12)。想定以上に売上げが出た医薬品について、単価を引き下げても新薬メーカーの収益確保は可能と見られます。
このことを踏まえて、医薬品費の引下げのために薬価を調整する目的でこの再算定が行われています。しかし、新薬メーカーの側は、売上げが増えると、薬価の切り下げにつながるため、イノベーションを阻害し、新薬開発の意欲が削がれるとして反対してきました。
(*12) 類似薬効比較方式で薬価が算定された新薬は、年商150億円超かつ実際の売上高が想定の2倍以上となった場合に、最大で15%薬価が引き下げとなります。原価計算方式で薬価が算定された新薬は、年商150億円超かつ実際の売上高が想定の2倍以上 又は 年商100億円超かつ実際の売上高が想定の10倍以上となった場合に、最大25%薬価が引き下げとなります。
(2) 特例拡大再算定
近年、一部の抗がん剤などで、服薬効果の高い、高額な医薬品が販売されました。医薬品の適用対象となるがんの病態の範囲が拡大され、対象の患者が増加したことにより、これらの医薬品の費用が医療費全体を押し上げて、医療財政を圧迫するとの懸念が生じてきました。
そこで、2016年に、「特例拡大再算定」と呼ばれる市場拡大再算定の巨額販売版(*13)が導入されました。2017年2月には、この特例拡大再算定によって、緊急的に、抗がん剤のオプジーボ(小野薬品工業社)に限って薬価を半額に引き下げる対応がとられました。
(*13) 年商1000億円超1500億円以下かつ実際の売上高が想定の1.5倍以上の場合は最大25%、年商1500億円超かつ実際の売上高が想定の1.3倍以上の場合は最大50%、薬価が引き下げとなります。
(3) 用法用量変化再算定
厚生労働大臣の承認を受けて、主たる効能または効果に関する用法と用量に変更がなされた医薬品は、薬価が再算定されます。2018年の薬価改定で、効能変更等に伴って用法と用量に大幅な変更がなされた医薬品については、市場規模が100 億円を超え、かつ、変更前に比べて10 倍以上となった場合に、薬価が再算定されることとなりました。オプジーボには、この再算定が適用されて、薬価がさらに引き下げられています(*14)。
今後、年4回の見直し時期が設けられ、再算定の対応がとられることとなっています。
(*14) 2018年度に、用法用量変化再算定と費用対効果の価格調整により、薬価はさらに23.8% ほど引き下げられています。
3|ジェネリックの促進に向けた価格体系が導入されています
日本では、特許期間切れとなった医薬品(長期収載品(*15))が、ジェネリック医薬品ほど価格が下がらないまま使用され続けることが、医療費削減が進まない要因の1つとされてきました。
そこで、ジェネリック医薬品が発売されて5年経過した薬価改定以降で、特例引き下げが行われています。引き下げ幅は、ジェネリック医薬品への置き換えの進み具合に応じて、定められています。2018年の薬価改定では、置き換え率が40%未満の長期収載品は、改定後の薬価から2%を差し引くことなどとされています(*16)。
また、ジェネリック医薬品が発売されて10年が経過した薬価改定以降は、長期収載品の薬価をジェネリック医薬品の薬価を基準に段階的に引き下げることとされています。
(*15) 薬価基準に長期間収載されている品目であるため、このように呼ばれています。
(*16) 置き換え率が40%以上60%未満の場合は1.75%、60%以上80%未満の場合は1.5%が差し引かれます。
4|費用対効果の考え方が試行的に導入されています
医薬品について、費用対効果を分析して、その結果に基づいて薬価の改定を行う仕組みが検討されてきました。2018年の薬価改定では、革新性が高く市場規模の大きい7つの医薬品(*17)について、費用対効果の評価結果に基づく価格調整が試行的に導入されています。
費用対効果の価格調整の大まかな考え方を、簡単に紹介します。
分析対象の新薬が、既存薬に比べて、どれだけ効果があり、どれだけ費用がかかるかを評価します。効果は、完全な健康状態に換算した場合の寿命(QALY (Quality-Adjusted Life Year, 質調整生存年))の伸びとします。一方、費用は、この価格調整を行う前の薬価をもとに計算する生涯公的医療費推計の増加分とします。
そして、費用を効果で割り算したものを、増分費用効果比(ICER (Incremental Cost-Effectiveness Ratio))と呼びます。ICERが高いほど、同じ効果を得るのに費用が多くかかることになります。
試行的に導入された価格調整では、ICERが500万円以下の場合、薬価の引き下げは行いません。500万円超1,000万円以下の場合、ICERが高いほど薬価の引き下げが大きくなります。ICERが1,000万円を超える場合、薬価のうち、価格調整対象部分の90%が引き下げとなります。
今後、将来の本格実施に向けた検討を進め、2018年度中に結論を得ることとされています(*18)。
薬価については、今後も制度見直しに関する議論が続いていくものとみられます。引き続き、その動向に注目していく必要があると考えられます。
(*17) 具体的には、C型慢性肝炎治療薬のソバルディ(ギリアド社)、ハーボニー(同)、ヴィキラックス(アッヴィ社)、ダクルインザ(ブリストル・マイヤーズ社)、スンベプラ(同)、抗がん剤のオプジーボ(小野薬品工業社)、カドサイラ(中外製薬社)です。なお、これとは別に6つの医療機器も費用対効果の試行的実施の対象とされています。
(*18) 費用対効果評価の結果は、価格調整に用いることとし、保険償還の可否の判断には用いないこととされています。
関連レポート
(2018年4月6日「基礎研レター」より転載)
株式会社ニッセイ基礎研究所
保険研究部 主任研究員
