■ "細菌"に思いを馳せて
寒い日が続くと、つい近所の焼き肉の芳香につられてしまい、ふらりとお店に入ってしまう。ホルモンをタレでいただき、舌に残った名残惜しさを、ビールと一緒に流し込む至福の時。バーベキューは楽しいが、お肉はしっかりと焼かなければ痛い目にあってしまう、と身をもって学んだ方々も多いのではないでしょうか。楽しい焼き肉パーティーも調理しだいで、「実弾」入りのロシアンルーレットの会と化してしまいます。
お肉が原因で食中毒症状が出た場合、病原性大腸菌が原因の一つだ、と今の私達は推測するでしょう。ただ、実際に細菌が原因で病気が引き起こされる、という知見を人類が得たのは、近代になってからでした。例えばペスト菌の大流行は6世紀のローマ帝国や14世紀の西ヨーロッパを襲撃し、人類史に大きな爪痕を残したと言われていますが、当時の人々には為す術なし。最新研究の理解を助けるためにも、少しだけ微生物学の進歩の歴史を振り返ってみましょう。
16 世紀には顕微鏡が発明され、肉眼で見えないものが可視化される時代に突入しました。時は流れ、1850 年には炭疽症にかかった羊から、細菌が分離されました。炭疽菌の純粋培養に成功したコッホ博士は、パスツール博士と並んで、微生物研究から始まる、生命科学発展の基礎を築いた一人です。1876 年には、博士は培養した炭疽菌を注入された動物が病気を発症することを、実証的に明らかにしました。
でも、たくさんの疑問が残ります。感染した個体が病気を発症するメカニズム・細菌の中で、毒性のあるものとそうでないものとの違い・細菌が個体に感染する機構など、わからないことだらけです。
細菌を使った人体実験は倫理上難しい(ピロリ菌を自ら飲みこんで、体を張った研究者もいらっしゃいますが)。漠然とした疑問を具体的で簡潔な問題に設定しなおし、研究者たちは遺伝子ハンティングに出かけて行きました。
1970 年代から90年代には、彼らは穴だらけの網をもって漁に繰り出し、非効率的な戦いを余儀なくされていた。今では精巧な網のおかげで獲物を一網打尽にしてしまう、「根こそぎ漁法」が主流です。網や漁場を変えることで、目的の獲物を手にするチャンスが得られます。
「漁場」をどこにしようか、「漁法」はどのようにしようか、と労働力コスト、時間・経費コストを加味しながら、「漁師」たちは考えます。これまでも、そしてこれからも、研究者独自の創意工夫が加わり、創造的な研究が行われていくことでしょう。
今回は、細菌(特に病原菌)の実態を捉えるために、研究者たちに採用された方法論に注目してみたいと思います。
■ 病原菌のワルサ(毒性)を、分子の言葉で説明する
細菌と宿主との関係を解明するために用いられる実験手法のアイデアを、模式図(図1)を使って簡単に説明してみましょう。
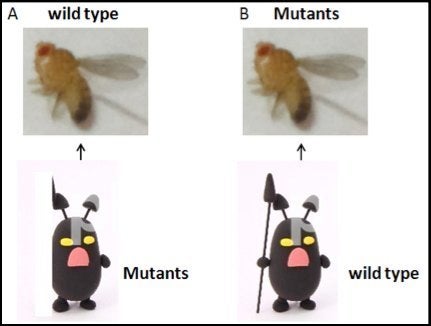
ハエに天敵の細菌がいたとしましょう。この細菌がもつ毒素や、ハエに感染する際に欠かせない機能を果たす遺伝子を同定したいのであれば、まず細菌の突然変異体を分離すればいいでしょう。そして、一つ一つの系統を培養し、野生型のハエに感染させてスクリーニングすればいい(図1A)。逆にハエの持つ免疫システムを明らかにしたいのであれば、ハエの突然変異体を用意して、細菌に対する抵抗性の変化に着目してスクリーニングすればいい(図1B)。双方向の研究を行うことにより、宿主と細菌との相互関係を、より広く理解することが可能となるのです。
■ 病原菌を科学する
1990 年代には、ランダムに無理やり外来遺伝子を細菌のゲノムに挿入させ、突然変異体を分離する技術が確立していました。外来遺伝子には、目印となる標識がついているので、どこに挿入されたかも後で確認することが可能でした。
「分離した何千株という細菌の突然変異体が、感染先の動物の体中でどう振舞うかを調べたい。動物を一対一で準備することは現実的に難しい。どうすればいいだろうか」
そのような中で、1995 年にロンドンのホールデン博士率いる研究グループが一つの解決策を提案しました。signature-tagged mutagenesis (STM) と名付けられた、標識付きの突然変異分離法(図2)です。STM 法は、簡単に言えば、実験室の人工的な培養条件下で生き残る細菌系統と、一度マウスに感染させた後、生体の組織で生き残っている細菌系統とを比較して、生体で生育できない細菌の系統を特定する手法です。いろいろな組み合わせで実験を行うことが可能です(両者ともに生体を経由してもいい)。
(A)
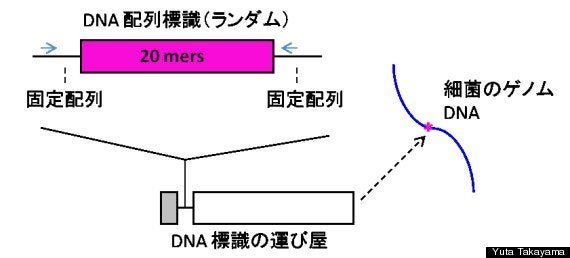
(B)
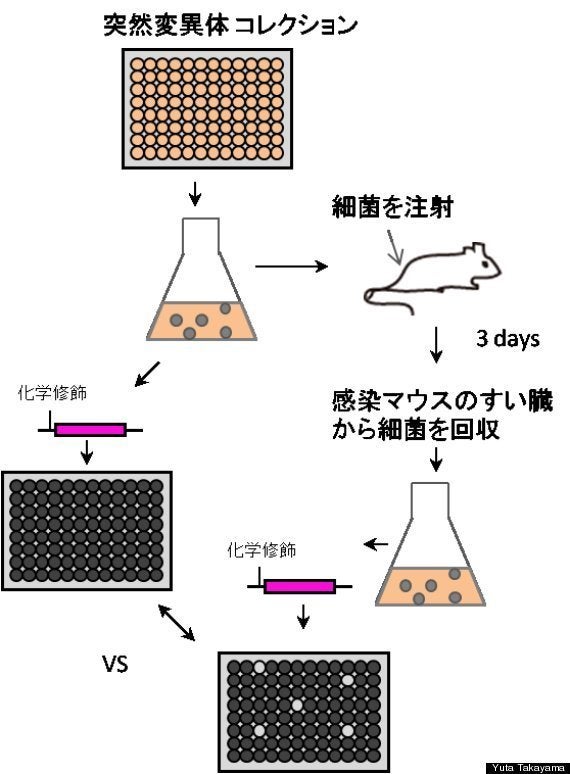
ホールデン博士らは、条件検討により、一匹のマウスに注射する系統数を割り出しました(96 種類)。打ちこむ種類が少なすぎると実験に必要なマウスが増えてしまい、コストが増大してしまう。しかし、多すぎても実験結果が上手く得られなくなるジレンマを抱える手法です(後述)。
■ 完璧な実験方法など存在しない
ある現象に注目し、その内在論理を解明するには、採用する方法論の利点と欠点とを熟知していなければ大やけどをしてしまう。研究室だけの話ではなく、どんなにすぐれた方法にも必ずや落とし穴がある、このことを頭の片隅においておくことは重要と思います(どんな人格者にも悪魔が宿っている)。論文に発表されている実際の写真を見てみましょう(図3)。
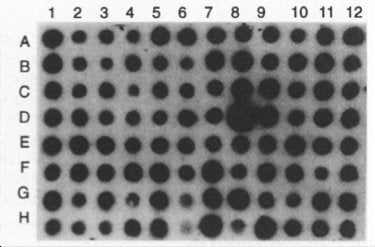
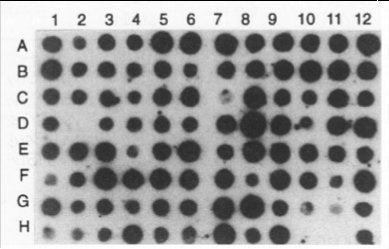
実際の写真を見ると、(B)で消えたかどうかの判定が難しい、と感じてしまう方もいらっしゃるでしょう。それでも見た目に分かりやすい手法で、スクリーニング手法として優れており、多くの研究者達に受け入れられている方法なのです。どのような欠点があるのでしょうか。
「 96 種類の突然変異体を同時に用いる場合、再現性の高い結果が得られるのだが、その倍 192 種類の突然変異体を用いた場合、検出されるシグナルが弱くなり、再現性に問題が生じてしまう」
このように、論文の中でホールデン博士らは語っています。問題点は次の2点に整理されます。
1)生体に打ち込む突然変異体の系統数が増えれば、検出感度以下のレベルで生存する細菌の割合が上昇してしまう。
これでは、突然変異体の候補系統がいたずらに増えてしまい、誤った情報を受け取ってしまう頻度が高まります。スクリーニングとして失敗です。
2) タグは一度、突然変異体の細菌集団から抽出したゲノム DNA を鋳型として、化学反応によって増幅する必要があります。系統数が増えれば増えるほど、検出に必要なレベルまでタグを増幅することが難しくなってしまう。
1)と2)の問題点を克服できる系統数として、ホールデン博士らは 96 種類に落ち着いたのでした(実験には 12、24、48、96 ウェルプレートが用いられることが多いので、このような中途半端な数字になっています)。
実は他にも注意すべき問題点があります。たとえば、ある一種類の突然変異体は、その系統単独では生体内で生存できないのに、他の系統の細菌と共存することにより、生体内で生存できてしまう場合があるのです。せっかくスクリーニングで重要な突然変異体を分離していたのに、見落としてしまう危険性があることも、心に留めておきたいものです。
完璧な実験手法など、この世には存在しない。複数の系を用いて、いろいろな角度からのアプローチを試みることにより、一つの実験手法では決して得ることができない知見を、人類は手にしてきたのです。このことを担保するのは、同じ現象に着目する研究グループが複数あり、それぞれが独立して、重複しつつもある程度お互いに相異なる手法を採用する、競争的な研究環境なのかもしれません。そして、得られた研究結果についても、じっくりと落ち着いて分析する必要があるのでしょう。
【参考文献】
