アスタチン(At)という元素をご存じでしょうか?・・・え、そんなの知らない!?まぁ無理もないでしょう。化学を専門とする筆者にしても、これまでの人生で一度もお目にかかったことがない元素です。
実にこれは希少中の希少である放射性ハロゲン元素です。その宿命として寿命が短く、研究はあまり進んでいません。性質は今もってほとんど謎に包まれています。
しかし最近になってこのアスタチン元素に、一つの応用が考えられつつあるようです。それは放射線療法です。
■ 放射線同位体(RI)内用療法とは?
ざっくり言うと、「放射性元素を含む化合物を投与し、体内から放射線で病巣細胞を攻撃する治療法」です。
・・・え、これは全身被曝じゃ無いのか!?やたらめったら細胞を攻撃するなんて危ないじゃないか!!・・・と思えるかも知れません。
しかしご安心ください。この目的で使われるのは飛程の短いβ線です。組織内で数ミリメートルしか飛ばないため、直接触れたりしない限り、体外からは浴びたくても浴びようがありません。そして勿論、放射性元素をそのまま投与するわけではありません。認識能を持つ化合物とくっつけて、病巣部位だけに集積させて使います。
この考えに基づく医薬の代表例として、90Y-ゼヴァリン(2002年に米国で上市)が知られています。β線放出核種である90Y(イットリウム90)を、抗CD20抗体にキレート担持させた形をしています。つまりは抗体医薬の一種です。
これは非ホジキンリンパ腫というがんの治療に有効とされています。抗体ががん細胞を認識し、そこに付随する放射性核種が壊変によってβ線を放出、これががん細胞細胞のみを集中攻撃します。β線の組織内飛程が適切なため、抗体結合部位の周りにあるがん細胞も攻撃でき、治療効果が増大します(クロスファイアー効果)。
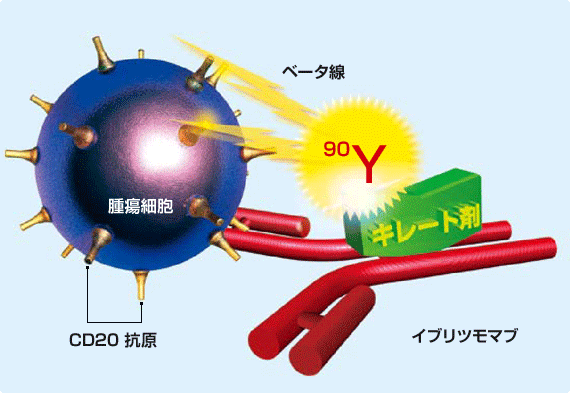
画像はこちらのサイトより引用
■ アルファ線をRI内用療法に応用する
使い方次第では薬にもなる放射線ですが、β線はエネルギーが低く、限られた治療以外には実用されていません。
より広汎な応用を目指す観点から、α線の利用も検討されつつあります[1]。こちらはβ線よりもさらに飛程が短い反面、線エネルギー付与率が高いという特徴が有ります。
このα線の特性により、腫瘍への局在がうまく行くなら正常組織への被曝を少なくできる、つまり副作用の軽減が見込めると考えられています。線エネルギー付与率が高いため、DNA二重鎖切断能や細胞殺傷力も大きくできます。また、放射線抵抗性を示す低酸素細胞や、感受性の低いS後期細胞にも有効だと考えられています。
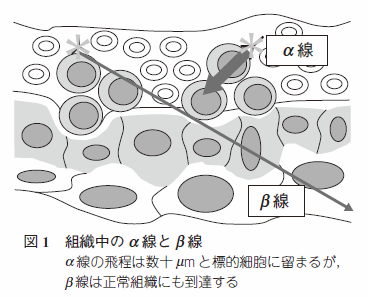
論文[1]より引用
たとえば223Ra(ラジウム223)から放出されるα線の組織中平均飛程は、100マイクロメートル以下とされています。これは細胞数個分の長さに相当するため、ごくごく近傍のみで効果を示すにとどまります。逆に言えば、いかにして病巣部にこれを集積させるかがカギとなります。
最近、ノルウェーのAlgeta社により、223Raが転移性骨腫瘍治療薬(商品名 Xofigo)として応用されました。2013年には米国で医薬承認を受けています。
アルカリ土類金属であるラジウムは、カルシウム主体の骨に親和性があります。投与によって骨代謝の亢進した転位部位にのみ集積し、腫瘍選択的な治療効果を示すとされています。
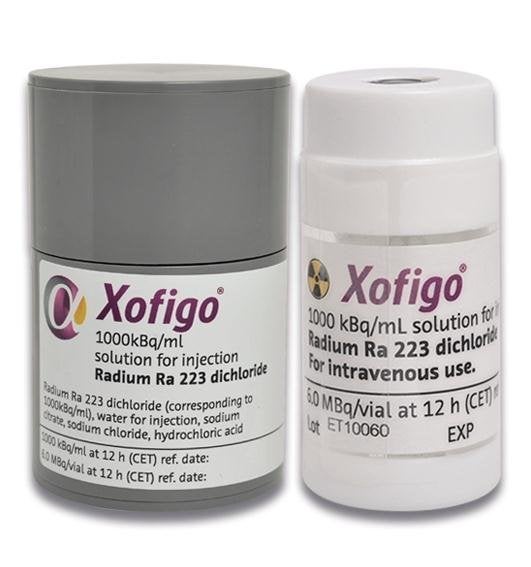
とはいえα線の飛程は短く、腫瘍細胞へ十分な線量が到達するかは疑問とされています。なぜ薬効があるのかについては、未解明の点も多く残されているようです。
■ アスタチンの利用
既に述べたとおり、α線放出核種は病巣付近に精密集積させてこそ効果を発揮します。より応用範囲を広げるには、認識能を担う抗体・小分子医薬に結合させておく必要があります。
しかしα線放出核種は一般に複数回の壊変を経るため、元素の物理化学的性質がたびたび変化します。つまり、キレートなどで安定担持を行うことが難しいという問題があるのです。
ここで満を持してアスタチンの登場です!!
211At(半減期:7.2時間、平均エネルギー:6.79 MeV、α線飛程:55-70μm)は、他のα線核種と違ってハロゲン元素であるため、安定な共有結合で医薬分子に導入できる特長を持っています。
また壊変は100%α線放出であり、γ線放出過程を含みません。このため他の核種よりも安全に取り扱えます。また、壊変途中の211Po X線を利用すればイメージングにも応用でき、体内動態を詳細に追える利点もあるようです。
さてこのアスタチン、どうやって医薬分子に導入すれば良いのでしょうか?
非常にマニアックな有機合成ですが、スズ試薬を用いた方法が知られるようです(下図)[3]。
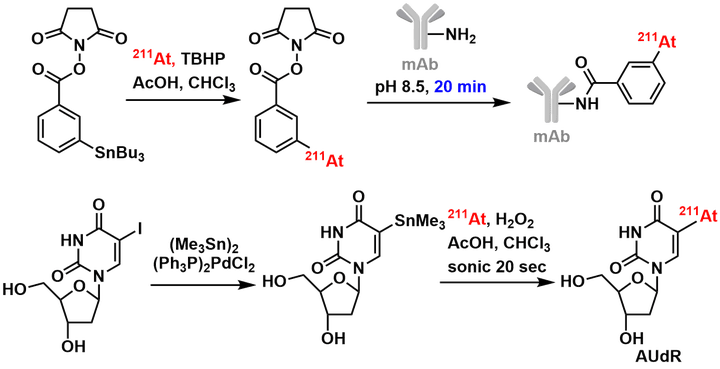
またこの方法で作ったアスタチン化抗体・小分子医薬を実際の治療へ使うべく、作業工程のオートメーション化なども検討されていようです[4]。
アスタチン導入オートメーション装置。グローブボックス内に設置する。j)が反応容器(論文[4]より)
アスタチン導入オートメーション装置。グローブボックス内に設置する。f)が化学反応容器(論文[4]より)
■ おわりに
現代の医薬開発は、難治性疾患を主標的としています。ともあれ病気さえ治れば・・・と手段を選ばなくなりつつあるのでしょうか。こんなものまで持ち出してくるのかよ!・・・というのがこのお話を知ったときの偽らざる第一印象ではありました。
アスタチンに限らず、RI内用療法では放射性核種を扱う化学変換が良く使われます。これには「半減期との競争」という問題が常につきまとっています。化合物を壊さず、高速・短時間で進行する反応開発研究は、こういった分野において需要があるといえます。普段なかなか思い付かない観点ではありますが、有機合成化学者にも貢献できることはありそうです。
ただ、アスタチンには安定同位体が存在しないため、常に放射性核種で反応検討を行う必要があるようです。患者の命を救うためなら、体を張るなんて何のその!・・・との信念を持てる人が、この辺りの分野を進歩させていく?のかもしれません。
放射線研究はこのWikipedia項目にも記されるがごとく、壮絶な逸話が満載ですが、アスタチンの世界もなかなかに壮絶と思えます・・・いかがでしょう?
■ 関連文献
"α線内用療法の現状と展望" 細野 眞、Isotope News 2013年7月号 No711 [PDF]
(a) "Enigmatic astatine" D. S. Wilber, Nat. Chem. 2013, 5, 246. doi:10.1038/nchem.1580 (b) 邦訳:謎めいた元素「アスタチン」
"Astatine-211 labeling: a study towards automatic production of astatinated antibodies" E. Aneheim; H. Jensen; P. Albertson; S. Lindegren, J. Radioanal. Nucl. Chem. 2015, 303, 979. DOI: 10.1007/s10967-014-3561-8
"Automated astatination of biomolecules - a stepping stone towards multicenter clinical trials" E. Aneheim; P. Albertsson; T. Bäck; H. Jensen; S. Palm; S. Lindegren, Sci. Rep. 2015, 5, 2025. DOI: 10.1038/srep12025
■ 関連動画
(2015年11月10日「Chem-Station (ケムステ)」)
