伊丹 健一郎氏、 山口 潤一郎氏
ベンゼン環は、有機化学の象徴ともいうべき構造であり、天然・人工を問わず多くの化合物の基本単位だ。このベンゼン環に各種の置換基を導入することで、多様な性質を引き出すことができ、例えば液晶材料・有機EL・医薬品などの高付加価値化合物がここから生み出される。このため、ベンゼン環上の望みの位置に必要な置換基を導入する手法の開発は、化学の黎明期から変わらぬ重要なテーマだ。このほど名古屋大学の伊丹健一郎教授、山口潤一郎准教授らのグループは、ベンゼン環の6つの炭素に、全て異なる芳香環が導入された「ヘキサアリールベンゼン」の合成に成功した。その意義、研究の経緯などを、両博士に伺った。


ターゲットは「カッコいい分子」
―― 今回の論文のテーマは、ヘキサアリールベンゼン(HAB、図1)の合成です。この化合物を合成ターゲットに選んだ理由は?
伊丹氏: 第一に、僕は「ベンゼンが好き」というのが根本にあります。美しい分子じゃないですか。そのベンゼンに、さらに6つもベンゼンがついているわけですから、好きな人にはたまりません(笑)。
山口氏: 僕も、構造式を見ただけで「ああ、これはあの人の仕事だな」と思ってもらえるような、カッコいい分子を作ってみたいという思いがありました。HABは、6つのベンゼン環がプロペラのようにねじれた3次元的な構造で、「自分の手で作ってみたい」と思える分子でした。
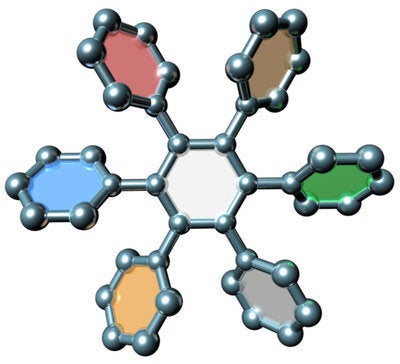
図1:ヘキサアリールベンゼン(HAB)
中央のベンゼン環に対して、6種の異なる芳香環が結合している。芳香環はサイズが大きいために互いに反発力が働き、効率よく導入することは難しい。さらに、周辺の置換基の組み合わせによって極めて多様な可能性があり得るため、目的のものだけを合成するのは非常に困難である。
―― 共通するのは、「カッコいい分子を作ってやろう!」という点ですね。
山口氏: 完全にそのとおりです(笑)。実験を担当した鈴木真君もカッコいいものが大好きなので、彼にはカッコいいテーマでないとダメだろうと。
伊丹氏: 我々の論文には「美しい構造」という言葉がよく出てくるので、共同研究をしている物理学の人などには、「化学者というのは皆『美しい』ことをそんなに重視するのか」と不思議がられたりします。
―― どの学問分野でも、「美しさ」というのは重要かと思えます。
伊丹氏: 我々は、「美しいものには機能が宿る」という信念を持って取り組んでいます。例えばHABは、我々の研究室の重要テーマであるナノグラフェンや、その他の各種高機能材料の合成に結び付きます。ただしそれ以上に、「破格の構造多様性」に挑むという目標がありました。
―― HABには極めて高い多様性がある?
伊丹氏: はい。6つの異なる置換基の組み合わせから考えられる置換ベンゼンの可能な分子数を計算してみると、置換基が6種類であれば4291種、20種なら537万以上、50種なら13億を超えます。この中には、素晴らしい機能を持つ分子があるはずですが、HABのこの多様性は現在もまるで活用できていないわけです。
「プログラム合成」で難物に挑む
伊丹氏: そこで、我々が以前から提唱している「プログラム合成」という概念で、この究極のターゲットに挑んでみようということになりました。
―― 論文のタイトルにも登場する言葉ですね。どういった概念ですか?
伊丹氏: 今まで、有機合成では「選択的合成」ということが重視されてきました。幾何異性体、光学異性体などさまざまな異性体の中から、欲しい1種だけを選んで作り出すということです。しかし、可能性のある分子全てを作り出すことができればもっといい。それも、1つ1つ違う方法で作るのではなく、単一のスキームで合成したいということです。これをプログラム合成と呼んでいて、選択的合成の上位概念になると考えています。
―― 多様な化合物群を、体系的、統一的に合成する手法ということですね。
伊丹氏: 最初にターゲットにしたのは、多置換オレフィンでした。オレフィンには4つの置換基が結合できますが、位置によって反応性が異なるので、これを利用して順次置換基を導入することで解決しました(図2)。多置換の各種ヘテロ環なども制覇していって、いよいよベンゼンに手を付けたのが2005年です。しかしこれは難しすぎ、2007年頃にいったん放棄しました。
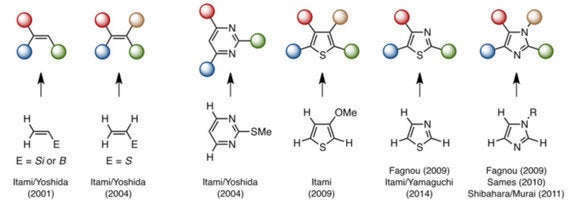
図2:多置換オレフィン・多置換ヘテロ環のプログラム合成
一置換オレフィンは対称性が低く、置換位置の環境が全て異なるため、比較的合成は容易。また、各種ヘテロ環は、窒素やイオウ原子の存在によって、置換位置の反応性が異なっているため、これを利用して選択的な置換基導入ができる。
―― ベンゼンはそんなに難しいのですか?
伊丹氏: ヘテロ環の炭素はそれぞれ環境が違いますが、ベンゼン環は対称性が高いので、炭素はほぼ同じ環境にあります。ですので、1カ所だけを狙って変換するのは至難の業です。
―― その難物に、再挑戦することになったきっかけは?
伊丹氏: 3年半ほど前、山口君が「僕らはHABにすごく近いところまで来てますよ」と言い出しまして。当時、チオフェンに4つのアリール基を導入する方法はすでに完成していました。これをベンゼン環に変換すればいいと。眼からうろこでした。このメンバーでなければ、生まれなかった研究です。
山口氏: チオフェンは有機導電体など機能性分子によく出てくる骨格ですが、合成屋である自分には、シンプルに4炭素のユニットに見えていました。これを、2炭素のユニットとDiels-Alder反応で結合させればベンゼン環になる、という単純な発想です(図3)。
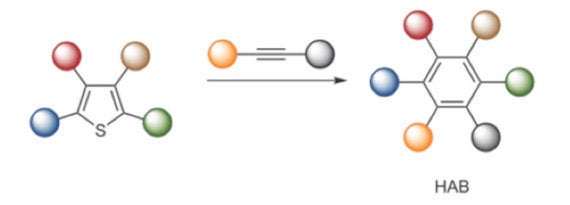
図3:HAB合成の基本概念
4つの異なる置換基を持ったチオフェン(左)と、非対称の二置換アセチレン(中央)を反応させることで、6つの異なる置換基を持ったHABが合成できると考えられる。
C-H結合活性化
―― その4置換チオフェンの合成には、C-H活性化反応が駆使されています(図1)。21世紀の大きなトレンドとなっているジャンルです。以前は、分子内にたくさん存在するC-H結合のうち、狙ったものだけを反応させることなど、なかなか考えられませんでした。
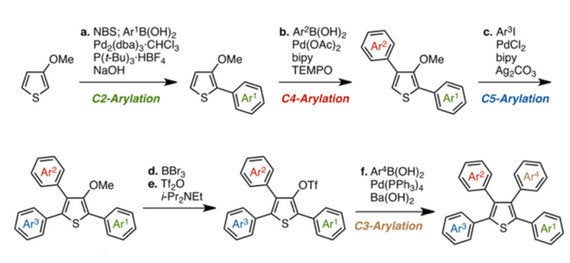
図4
4置換チオフェンの合成。メトキシ基(-OMe)を足掛かりに、チオフェン環上に順次アリール基(Ar)を導入していく。Ar、Ar、Arの3つのアリール基が、C-H結合活性化反応によって導入されている。
伊丹氏: 大きなきっかけになったのは、村井真二先生が1993年に報告した反応です(参考文献1)。それまでは、「こんなことができるはずがない」と、心理的な障壁が高かったのだと思います。しかし「こういうことができる」と分かってからは、多くの研究者が参入して一挙に研究が進みました。
―― C-H結合活性化が与えた影響は大きい?
伊丹氏: 複雑な分子の合成工程は、以前に比べて半分くらいになったのではないでしょうか。コストや廃棄物は、合成工程数に依存しますから、非常に大きな変革です。
―― さて次は、そうして作った四置換チオフェンを、ベンゼンにする段階です。
山口氏: チオフェンそのままでは、Diels-Alder反応を受けつけないのは常識です。ただ僕は、このような芳香環を壊すこともテーマとしていましたので、チオフェン環を酸化してS-オキシドにすることで芳香族性をなくし、ジエンとして反応させる着想はすぐに出てきました。これをジアリールアセチレンと一緒に加熱するとDiels-Alder反応が進行し、一酸化硫黄の脱離を伴ってHABの骨格が出来上がります(図5)。
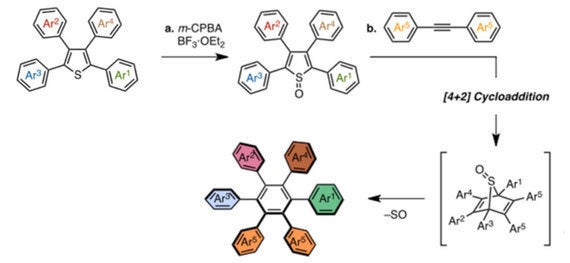
図5
チオフェン骨格は芳香族性を持ち、安定で反応しにくい。そこで、イオウ原子を酸化してS-オキシドにすると、芳香族性を失ってジエンとしての性質を帯び、Diels-Alder反応を受け付けるようになる。反応後、一酸化イオウ(SO)が脱離してゆき、HAB骨格が出来上がる。
―― ただ、このDiels-Alder反応は位置選択性が出ないのですね。
山口氏: 基質が両方ともほぼ対称的な分子なので、こればかりはちょっとどうしようもありません。
伊丹氏: ただ、何億という可能性の中から2つにまで絞り込んだわけです。これをどうにか分離できれば、世界で誰も果たしたことのないHABを手にすることができますので。
山口氏: この構造決定がまた難航しました。X線結晶解析をしてみたところ、対称性の高い基本骨格ですので、ディスオーダー(結晶内での分子の配向の乱れ)を起こして、解析がうまく行かなかったんです。
―― どう解決されたのですか?
山口氏: ケトン部分を還元して大きな置換基を結合させ、その部分をトリガーにして分子が積み重なるよう考えました。よい置換基を鈴木君が探し出してくれました。彼は持っていますね。
―― この研究で、いちばん嬉しかった瞬間ですか?
伊丹氏: それはもう(笑)。日付まで覚えていて、2014年7月31日ですね。鈴木君がX線結晶解析の図を持ってきた時、思わず「ギャーッ」と声が出ました。興奮しました。プリントアウトして今も壁に貼ってあります(図6)。
山口氏: 廊下の向こうの実験室にまで、先生の「ギャーッ」が聞こえてきましたよ(笑)。
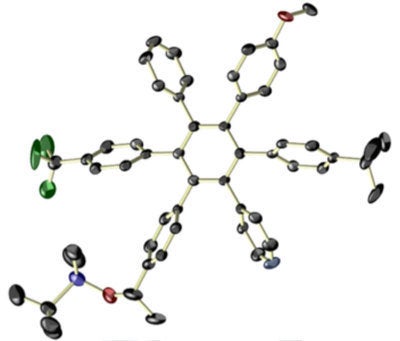
図6:HABのX線結晶解析図
6つの異なる芳香環が結合している。左下に、結晶化のための置換基(tert-ブチルジメチルシリル基)が導入されている。
―― やはり研究人生の中でも、そうはない瞬間でしょうか。
伊丹氏: シクロパラフェニレンやワープドナノグラフェンができた時ももちろん嬉しかったですが、叫ぶことはそうないですね(笑)。これからも何度か、叫ぶ日が来ると思いますけど。
分子で答えを出す
―― 論文発表後、さらに進展はありますか?
伊丹氏: ナフタレンやアントラセンなどに多数のアリール基が結合した、ポリアリールアセン類の合成が進んでいます。鈴木君はこの研究のために、就職がすでに決まっていたのを断り、博士課程に進学することになりました。「化学が好きで、今この研究をやらなかったら一生後悔する」と言ったら、会社も理解してくれて「では3年待ちます」と。
―― なるほど。伺っておりますと、非常に魅力ある研究室を作り上げていると思いますが、運営など気を配っていることはありますか?
伊丹氏: 僕1人がどうこうではなく、各自が「いい仕事をしよう、歴史に残る研究をしよう」という意識を持ってくれています。学生たちは、化学に対して真剣すぎるくらい真剣で、それが学生実験などを通じて代々伝わっています。僕は、ワイワイ言いながら一緒に楽しんでいるだけです。
山口氏: 伊丹研には、「朝は9時半に来る」こと以外に規則がないのです。僕自身も縛られるのが嫌ですし、本当に優秀な学生でしたら自発的にやってくれます。心底から化学を楽しみ、しかも真剣に取り組んでいると、そういう学生が自然に集まってきます。よいスパイラルが回ってくれていますね。
―― なるほど。伊丹先生は自分の研究室だけでなく、トランスフォーマティブ生命分子研究所(ITbM)の拠点長として、反応開発、ナノカーボン、植物ホルモンなど、多彩な分野で共同研究を進めておられます。
伊丹氏: 知らないことばかりで、日々勉強ですが、純粋に心躍らされます。新しい建物では、研究室同士の壁も全くなく、自由に行き来しながら実験をしています。こうした環境は、企業の方も見学に来ていますよ。そうした中でお互いワイワイやることで、用語の違い、文化の違いを越えられると思っています。そして他ジャンルの期待に応えて活躍する分子を創る、「分子で答えを出す」ことが、我々の目指すところです。
―― ところで、今回の論文をNature Chemistry 誌に投稿したのは?
伊丹氏: 皆が見てくれるジャーナルということで、当然の選択でした。こだわりがある論文は、やはり人の目に触れてほしいですので。
山口氏: よい位置付けの雑誌ですね。伝統のあるジャーナルなのにウェブ展開で先行していること、ニュースなど二次情報にも力が入っていることなど、素晴らしいと思います。
―― 最後に、今後の目標などお願いします。
伊丹氏: 僕は、分子の力を信じています。美しくて、あっと驚くような分子を今後も送り出したい。合成化学は無限で、絶対に終わることがないと思っています。
山口氏: 世界の研究者はもちろん、自分自身が魅了されるような分子を作りたいです。今後いろいろな研究に手を染めると思いますが、「分子を合成する」という主軸は変わらないと思います。世界を変えるような分子を思いついても、それを実際に作れなければ意味がありませんから。
聞き手 佐藤 健太郎(サイエンスライター)
(参考文献):
- Murai S. et al. Nature366, 529-531 (1993).
Nature Chemistry 掲載論文
「プログラム合成法によって可能になった5または6種の異なる置換基を持つヘキサアリールベンゼンの合成と性質解明」
Nature Chemistry7 227-233 (2015) doi:10.1038/nchem.2174 | Published online 26 January 2015
Author Profile
伊丹 健一郎(Ph.D.)
1998年京都大学大学院工学研究科博士後期課程修了
1998年京都大学大学院工学研究科 助手
2005年名古屋大学物質科学国際研究センター 准教授
2008年名古屋大学大学院理学研究科 教授(現在に至る)
2012年名古屋大学トランスフォーマティブ生命分子研究所 拠点長(現在に至る)
2013年JST-ERATO伊丹分子ナノカーボンプロジェクト 研究総括(現在に至る)
山口 潤一郎(Ph.D.)
2007年東京理科大学大学院工学研究科博士後期課程修了
2007年スクリプス研究所化学科 博士研究員
2008年名古屋大学大学院理学研究科 助教
2012年名古屋大学大学院理学研究科 准教授(現在に至る)
【関連記事】
