アルカリ金属を水に入れると派手に爆発する。化学の授業でおなじみのこの実験の反応機構が、実は長く誤解されてきたことが、ハイスピードカメラを使った研究で判明した。
なぜナトリウムは爆発するのか?謎解明!
Philip Mason/Czech Academy of Sciences
金属ナトリウムや金属カリウムの塊を水中に投げ入れ、爆発を眺める。化学を使った悪ふざけの定番ともいえるこの爆発反応は、アルカリ金属の高い反応性を説明する実験として、何世代にもわたり化学を学ぶ学生たちを驚嘆させてきた。ところが今回、これまで単純明快とされてきたその反応機構の裏に、一連の興味深いプロセスが隠されていたことが明らかになった1。
アルカリ金属が水と接触して起こる爆発は、金属と水との反応で発生した水素ガスが、同じく反応で生じた熱によって発火することに起因する、と長く考えられてきた。しかし、チェコ共和国科学アカデミー(プラハ)のPavel Jungwirthらを中心とする研究チームはこのたび、この爆発がこうした単純な化学反応でなく、金属からの電子放出と内部に残された陽イオンの電気的反発という意外な現象によって引き起こされることを発見し、Nature Chemistryに報告した(参考文献1)。
神経科医で化学愛好家でもある、著名な作家オリヴァー・サックスは、著書『Uncle Tungsten』(邦訳『タングステンおじさん』 参考文献2)でこの現象を「ものすごい化学現象」と称し、その様子をこう書いている。「たちまち火がついたナトリウムは、狂った流れ星のように水面を駆けずりまわり、辺り一面を黄色い炎の海にした」。
金属ナトリウムは室温では銀白色の固体で、ナイフで切れるほど軟らかく、水との接触で水酸化ナトリウムと水素を生じる。金属カリウムも同様に軟らかく、室温で銀白色の固体となるが、水とはナトリウムよりも激しく反応して水酸化カリウムと水素を生じる。これらの反応は大量の熱を放つため、発生した水素が発火して爆発すると考えるのは自然なことだろう。
化学反応が暴走して爆発を起こすには、反応物質同士が迅速に効率よく混ざり合わなければならない、とJungwirthは説明する。しかし、アルカリ金属と水の反応では水素の他に水蒸気も発生するため、金属表面がこれらの気体で覆われて、水との接触が物理的に妨げられてしまうはずだ。金属表面に水が接触しなくなれば、金属は「燃料」を絶たれ、反応は次第に衰えていくだろう。だが、実際はそうはならない。それはなぜなのか?
この謎を解明すべく、Jungwirthの研究室に所属するPhilip Masonは、危険を承知の上で実験に挑んだ。実際に彼は、火を吹き消そうとフェイスシールドを外した際、金属片が顔に飛んできて、頬に擦り傷を負ったこともあったという。
アルカリ金属と水の反応は不規則で、さまざまな要因に左右される。Masonらは、こうした不確実性を取り除き、再現可能な方法で爆発の様子を観察することのできる実験手法を模索した。ナトリウムは空気に触れると表面が酸化されて爆発しなくなることがある。そこでMasonは、反応を確実にするため、室温で液体となるナトリウム‐カリウム合金を使うことにした。この合金をシリンジに入れ、不活性ガスであるアルゴンを満たした長さ1mのガラス管の上部から定量を滴下し、ガラス管の底にためた純水中に落下させることで、金属液滴の落下距離や速度など全ての条件を一定に保った。そして、この様子を約100マイクロ秒(μs)という時間分解能を有するハイスピードカメラで撮影したところ、「反応の初期段階で何が起きているのか」を解明する重要な手掛かりが得られた。
まず、シリンジから滴下した金属液滴が水に触れてからわずか0.3~0.4ミリ秒(ms)後に、液滴から針状の金属「スパイク」が無数に飛び出す様子が観察された。このスパイク発射は、化学反応で生じた水素ガスや熱に起因するとは考えられないほどの高速で起こる。また、スパイクを形成しているさなかの金属液滴の周囲で溶液が青紫色に変わっていたことも明らかになった。
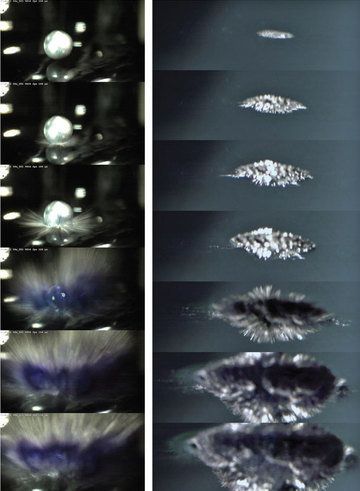
ナトリウム‐カリウム合金の液滴が水中に落下する様子。左側は水面を斜め上から、右側は水面を斜め下から捉えた画像。金属液滴が水面に触れた直後、超高速でスパイクが形成されている様子が見て取れる。また、スパイクが成長していく過程では液滴周囲の溶液が青紫色に変化している。(参考文献1)
これらの現象は、Masonと同じくJungwirth研究室に所属するFrank Uhligが行ったコンピューターシミュレーションの結果で説明できる。19個のナトリウム原子からなるクラスターをモデルとして第一原理分子動力学シミュレーションを行ったところ、クラスター表面の各ナトリウム原子が、水との接触から数ピコ秒(ps)以内に電子を1個ずつ失い、これらの電子が周囲の水へと飛び出して、溶媒和される(水分子に囲まれる)ことが分かったのだ(参考文献3)。
水中で溶媒和された電子(水和電子)は、藍色を呈することが知られており、今回観察された青紫色の溶液は、金属液滴周辺に水和電子が存在することを示している。一方、電子を大量に放出した金属クラスターの内部には多くの陽イオンが取り残され、これらの陽イオン同士が強いクーロン力(静電力)によって互いに反発・解離することで「クーロン爆発」が起こり、クラスターは炸裂する。ハイスピードカメラが捉えたスパイクの正体は、クーロン爆発の様子だったのだ。
電子の移動に始まるこうした一連の現象は、金属液滴が水に触れてから1msもしないうちに完了し、その後は金属と水との化学反応に移行する。そしてクーロン爆発により形成された無数のスパイクが金属の表面積を著しく増やすことで、水との反応を暴走させてガスを発生させ、激しい爆発につながるのである。
Nature ダイジェスト Vol. 12 No. 4 | doi : 10.1038/ndigest.2015.150403
原文:Nature (2015-01-26) | doi: 10.1038/nature.2015.16771 | Sodium's explosive secrets revealed
Philip Ball
参考文献
1. Mason, P. E. et al. Nature Chem.http://dx.doi.org/10.1038/nchem.2161 (2015).
2. Sacks, O. Uncle Tungsten 123 (Picador, London, 2001).
3. Young, R. M. & Neumark, D. M. Chem. Rev. 112, 5553-5577 (2012).
【関連記事】
Nature ダイジェスト Vol. 12 No. 410.1038/ndigest.2015.150412
Nature ダイジェスト Vol. 12 No. 410.1038/ndigest.2015.150430
